【錯誤】網傳「高端疫苗,5月12日還在招募65歲以上受試者參與二期臨床試驗,表定要做到9月30日。然後今天就硬幹了。要嘛是7月底施打二期都做不完全的疫苗,要嘛是拖到至少10月才有僅做完二期的疫苗」?
【錯誤】網傳「高端疫苗,5月12日還在招募65歲以上受試者參與二期臨床試驗,表定要做到9月30日。然後今天就硬幹了。要嘛是7月底施打二期都做不完全的疫苗,要嘛是拖到至少10月才有僅做完二期的疫苗」?
經查:
【報告將隨時更新 2021/6/4版】
一、專家指出,高端新冠疫苗第二期臨床試驗主試驗收案達3700人,已在2021年5月27日收集完所有研究數據和需檢驗抗體的血清,送交獨立資料處理單位解盲,將依此結果送交食藥署,由食藥署召集專家審查評估是否給予緊急使用授權。傳言所稱5月12日收案的臨床試驗,與第二期主試驗無關。
二、專家指出,高端在2021年5月12日公告之試驗計畫為第二期的次要實驗,是針對高齡族群給予中劑量及高劑量疫苗。高端第二期主要試驗已涵蓋2成高齡族群,實驗劑量為中劑量。次要試驗在主試驗未解盲就展開,是為了縮減解盲後若需做高劑量實驗的等待時間。
三、專家表示,二期臨床試驗針對不同族群、不同劑量有次要實驗設計,是常見且正常的事情。
傳言誤導實驗之公告訊息,並稱「高端疫苗第二期試驗還沒做完就硬幹」,因此,為錯誤訊息。
【查核聲明】相關資訊若有更新,本報告亦會同步更新。
背景
社群平台在2021年5月30日流傳一則訊息:「Medigen MVC就是高端疫苗,5月12日還在招募65歲以上受試者參與二期臨床試驗,表定要做到9月30日。然後今天就硬幹了。要嘛是7月底施打二期都做不完全的疫苗,要嘛是拖到至少10月才有僅做完二期的疫苗。這不是草菅人命,真的不是!草菅人命的本質是輕忽,這是殺人。」
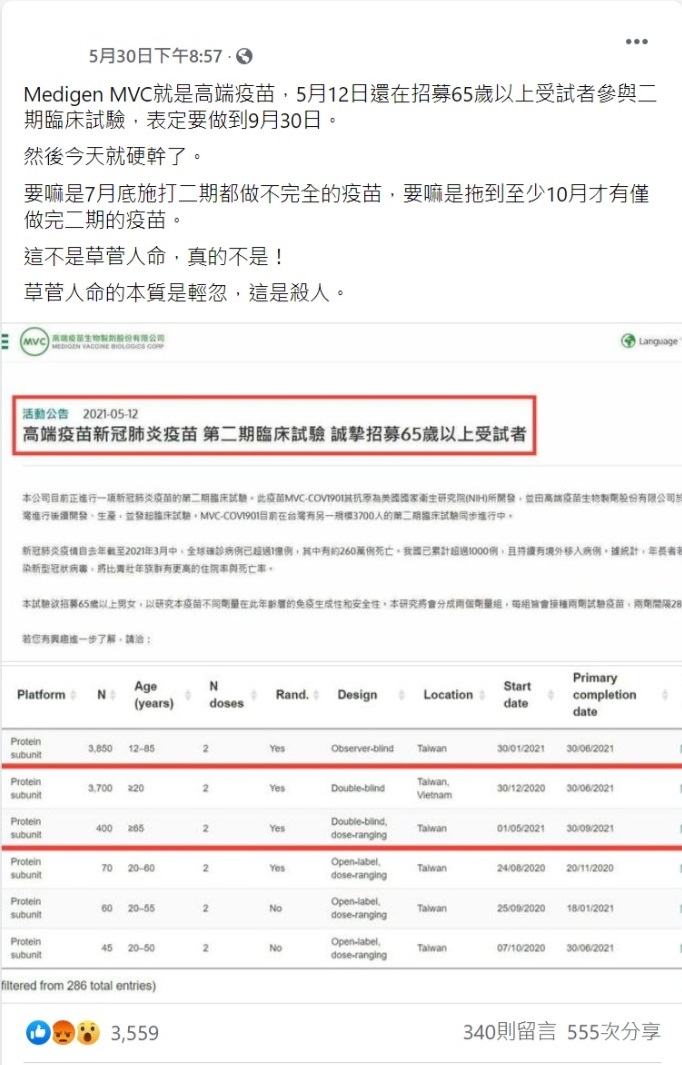
圖1:社群平台傳言擷圖
圖2:社群平台傳言擷圖
查核
爭議點一、傳言所提「高端公司二期臨床試驗,招募65歲以上受試者」公告,是否屬實?公告內容為何?
(一)查核中心檢視高端疫苗生物製劑股份有限公司網站,官網於2021年5月12日發佈公告,標題為「高端疫苗新冠肺炎疫苗 第二期臨床試驗 誠摯招募65歲以上受試者」,與社群平台傳言所附擷圖相同。
查核中心比對公告與網傳擷圖,標題已另加註(此為評估高劑量反應之獨立二期臨床試驗),但無法確知更新時間。

圖3:高端公司的活動公告擷圖
(二)查核中心諮詢國產新冠疫苗臨床試驗計畫主持人、臺大醫院感染科主治醫師謝思民。他表示,高端新冠疫苗第二期臨床主試驗是從2021年1月份開始執行,做到5月27日。共收案3700名成年人,其中包含2成(約800人)的年長族群,在5月27日已經收集完所有安全性資料和要檢測中和抗體的血液檢體,送出資料交由獨立資料處理單位解盲。意即高端新冠疫苗二期的主要試驗已經準備解盲。
謝思民說,第二期主試驗跟傳言所提5月12日仍招收高齡受試族群的次要實驗,並不相同,外界不應混為一談。
綜合以上,高端疫苗的第二期主試驗已於5月27日,收案3700名受測者資料,並送交公正單位準備解盲,而網傳所提的5月12日實驗,為第二期的次要實驗。
爭議點二、網傳「高端疫苗,5月12日還在招募65歲以上受試者參與二期臨床試驗,表定要做到9月30日。然後今天就硬幹了。要嘛是7月底施打二期都做不完全的疫苗,要嘛是拖到至少10月才有僅做完二期的疫苗」,是否屬實?高端的第二期實驗是否完成,可向食藥署申請緊急使用授權?
查核中心採訪衛福部食藥署。食藥署表示,食藥署在2020年12月29日核准高端執行第二期臨床試驗,該試驗主要收納成年人,高端國產疫苗主要的第二期臨床試驗目前已完成受試者收案及施打。
食藥署說,高端疫苗的臨床試驗結果、製程管控及藥毒理試驗等資料,仍需經過嚴謹專家審查,以確認疫苗的品質、安全及有效性後,才會核准其緊急使用授權。
食藥署表示,國內疫情環境難以執行大規模評估疫苗保護力的臨床試驗,經專家會議討論,考量科學理論基礎及風險利益評估,因此要求為:第二期臨床試驗收納至少 3500 ⼈以上受試者,以偵測發⽣率千分之⼀的不常⾒不良反應,以符合國際間對疫苗安全性的審查標準,並以免疫原性資料作為支持疫苗療效的佐證資料。
綜合以上,高端疫苗已在5月27日完成第二期試驗,食藥署將依據公正單位檢測結果,再送交給專家審查,確認疫苗各指標,才會決定是否核准其緊急使用權。網傳「以5月12日實驗,指出第二期尚未完成」是誤解其次要實驗之設計,與事實不相符。
爭議點三、高端公司在5月12日仍招募受測者的實驗用意為何?
(一)謝思民說,原本可以等高端疫苗第二期臨床試驗研究都解盲,看看中劑量對年長者是否產生足夠保護力,若保護力不夠,再追加進行高劑量的實驗。不過,食藥署擔心,面對險峻疫情,若要等解盲後才動作,可能延誤時程,趕不上病毒攻勢,因此要求在第二期臨床結束前,盡快展開年長族群的高劑量臨床試驗。
謝思民說,高端5月12日發出公告招募高齡受試者的試驗,是針對65歲以上族群,想比較中劑量及高劑量疫苗的保護效果。在第一期臨床試驗時,設計3種劑量,經實驗發現,中劑量效果就夠好,因此,第二期臨床以中劑量為主要劑量。不過,就像流感疫苗一樣,年長者可能對疫苗的免疫反應性比較差,除了中劑量外,也需考慮需要高劑量的可能性。
謝思民解釋,針對年長者的這個新試驗,是另一個獨立的臨床試驗,跟準備解盲的第二期臨床試驗,試驗單位不一樣、受試者也完全不同、試驗目標也不同,要做的是中劑量跟高劑量在年長族群的比較。總計收400人,隨機分派兩組,300人打高劑量、100人打中劑量。如果屆時二期主要試驗解盲後發現,年長者用中劑量疫苗就可產生足夠的中和抗體效價,或許就不需要使用高劑量。
(二)查核中心採訪國產新冠疫苗臨床試驗計畫主持人、雙和醫院血液腫瘤科主治醫師鄭偉宏。他表示,高端5月12日發出公告打算招募年長受試者的臨床試驗,與目前已經完成的第二期臨床試驗主計畫不相關。
鄭偉宏說,5月12日公告的臨床試驗是另一個獨立試驗,是針對年長族群,給予中或高劑量疫苗,看看高劑量是否能發揮更好的效果。因為一般認為年長者對疫苗的反應可能會差一些,先前第二期臨床試驗是給予中劑量,因此需要另一個實驗來嘗試看看,高劑量是不是可能帶來更好的幫助。
(三)查核中心諮詢台大公共衛生學院教授陳秀熙。他指出,各種族群對疫苗的免疫原性可能不同,臨床試驗的設計本來就會針對不同族群、不同劑量進行實驗,在各類實驗都經常看到這樣的設計,因此高端在主要的第二期臨床試驗外,額外再做其他族群的實驗,是很正常的事情。
(四)食藥署指出,網路傳言提到高端在2021年5月12日活動公告提到的試驗為不同的試驗計畫。網路傳言所提,針對年長者的第二期臨床試驗,是食藥署在2021年5月6日核准執行老年人第二期次要臨床試驗。此試驗⽬的是為進⼀步探討疫苗在老年族群的免疫⽣成性及安全性。
綜合以上,高端在5月12日開始招募年長受試者的二期臨床試驗是另一次要實驗,用意為縮短二期主試驗解盲後,若發現中劑量對長者保護力不彰而需重新試驗高劑量的等待時間。
結論
【報告將隨時更新 2021/6/4版】
一、專家指出,高端新冠疫苗第二期臨床試驗主試驗收案達3700人,已在2021年5月27日收集完所有研究數據和需檢驗抗體的血清,送交獨立資料處理單位解盲,將依此結果送交食藥署,由食藥署召集專家審查評估是否給予緊急使用授權。傳言所稱5月12日收案的臨床試驗,與第二期主試驗無關。
二、專家指出,高端在2021年5月12日公告之試驗計畫為第二期的次要實驗,是針對高齡族群給予中劑量及高劑量疫苗。高端第二期主要試驗已涵蓋2成高齡族群,實驗劑量為中劑量。次要試驗在主試驗未解盲就展開,是為了縮減解盲後若需做高劑量實驗的等待時間。
三、專家表示,二期臨床試驗針對不同族群、不同劑量有次要實驗設計,是常見且正常的事情。
傳言誤導實驗之公告訊息,並稱「高端疫苗第二期試驗還沒做完就硬幹」,因此,為錯誤訊息。
【查核聲明】相關資訊若有更新,本報告亦會同步更新。














